Một loại vaccine ung thư có sẵn có thể giúp ngăn ngừa tái phát bệnh ở bệnh nhân mắc hai loại ung thư nguy hiểm và tăng nhanh nhất trên thế giới. Loại vaccine này được thiết kế cho bệnh nhân có biến đổi gen KRAS, chiếm tới 90% số ca mắc bệnh. Một nghiên cứu sơ bộ đã kiểm tra hiệu quả của loại vaccine này ở người mắc ung thư ruột kết và tuyến tụy.
Tóm tắt nội dung chính
- Loại vaccine này sử dụng hai peptit để gắn với protein albumin, giúp vaccine đi thẳng đến hạch bạch huyết và kích hoạt hệ miễn dịch.
- Khi được tiêm liều cao nhất, 100% bệnh nhân có phản ứng miễn dịch, cho thấy vaccine có thể giúp giảm các chỉ số ung thư trong máu của bệnh nhân có dấu hiệu bệnh vẫn còn.
- Loại vaccine này là loại “sẵn có”, không cần được tùy biến cho từng bệnh nhân, do đó có thể tiết kiệm thời gian và chi phí.
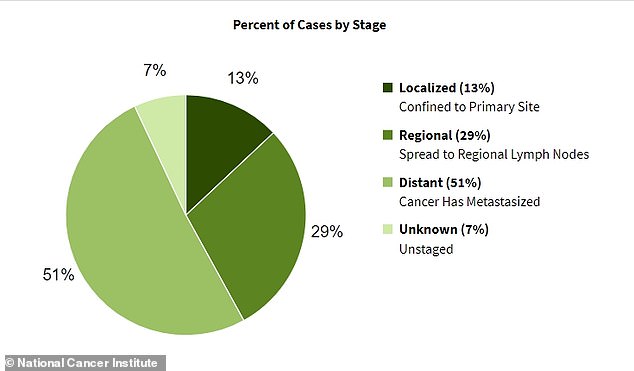
- Loại vaccine này chỉ dành cho bệnh nhân có ung thư chưa lan rộng, không áp dụng cho giai đoạn III hoặc IV của bệnh.
- Nghiên cứu này vẫn cần được xác nhận, nhưng các nhà nghiên cứu đã bắt đầu tuyển dụng hàng trăm bệnh nhân cho giai đoạn tiếp theo.
Vaccine hứa hẹn điều trị hai loại ung thư nguy hiểm và tăng nhanh nhất
Một loại vaccine ung thư có sẵn có thể giúp ngăn ngừa tái phát bệnh ở bệnh nhân mắc hai loại ung thư nguy hiểm và tăng nhanh nhất trên thế giới.
Loại vaccine này được thiết kế cho bệnh nhân có biến đổi gen KRAS, chiếm tới 90% số ca mắc bệnh.
Một nghiên cứu sơ bộ đã kiểm tra hiệu quả của loại vaccine này ở người mắc ung thư ruột kết và tuyến tụy. Nghiên cứu đầu tiên trên người này cho thấy loại vaccine, được phát triển bởi công ty nhỏ Elicio Therapeutics, có khả năng giảm nguy cơ tái phát bệnh ở 100% bệnh nhân đã phẫu thuật cắt bỏ khối u nhưng vẫn có các chỉ số ung thư trong máu.
Mặc dù đã cắt bỏ khối u và không có dấu hiệu của bệnh trên các chụp ảnh, gần như tất cả các bệnh nhân đều có dấu hiệu của việc khối u quay trở lại vào lúc bắt đầu nghiên cứu.
Các nhà khoa học chạy nghiên cứu cho DailyMail.com biết rằng, mặc dù cần có nhiều nghiên cứu lớn hơn để xác nhận hiệu quả của nó, loại vaccine này có thể cải thiện tỷ lệ sống sót cho ung thư ruột kết, dự kiến sẽ là nguyên nhân gây tử vong số một do ung thư vào năm 2030, và ung thư tuyến tụy, chỉ có 12,5% sống sót sau năm năm.
Khác với các loại vaccine ung thư thử nghiệm khác đang được phát triển, loại vaccine này sẽ không phải được tùy biến cho từng bệnh nhân, do đó có thể sẵn sàng hơn và ít tốn kém hơn.
Cơ chế hoạt động của vaccine

Loại vaccine này sử dụng hai peptit, G12D và G12R. Chúng gắn với albumin, một protein trong cơ thể giúp vận chuyển axit béo đến hạch bạch huyết. Albumin giúp vaccine đi thẳng đến hạch bạch huyết, kích hoạt hệ miễn dịch.
Điều này khác với các loại vaccine peptit khác, tiến sĩ Pashtoon Kasi, giám đốc nghiên cứu ung thư ruột kết tại Weill Cornell Medicine và một trong những tác giả của nghiên cứu cho DailyMail.com biết, vì các loại vaccine tương tự theo một con đường vòng vèo hơn, đi qua các cơ quan không cần thiết và bị phân hủy trong quá trình đó.
“Albumin được gắn vào nó giống như một con tàu vũ trụ hạ cánh trên một hành tinh. Nó buộc vaccine phải hạ cánh trên hạch bạch huyết,” ông nói.
Các peptit sau đó tạo ra một loại bạch cầu được gọi là tế bào T để chống lại các dấu hiệu ung thư còn lại.
Viện Ung thư Quốc gia ước tính rằng chỉ hơn 44% bệnh nhân ung thư tuyến tụy sống sót hơn năm năm nếu bệnh vẫn còn ở khu vực ban đầu. Nó có tỷ lệ sống sót trung bình là 12%
Đa số các ca ung thư tuyến tụy được chẩn đoán khi bệnh đã lan rộng đến nhiều cơ quan khác. Từ đó, bệnh trở nên khó điều trị hơn
“Chúng tôi đã phát hiện ra rằng hệ thống này có một lợi thế rất lớn,” tiến sĩ Christopher Haqq, trưởng phòng nghiên cứu và phát triển và giám đốc y khoa tại Elicio Therapeutics, công ty phát triển loại vaccine này, cho DailyMail.com biết.
“Nó không chỉ tạo ra số lượng lớn hơn của tế bào T, mà còn làm cho chức năng của tế bào T được cải thiện, chẳng hạn như khả năng xâm nhập vào khối u rắn, nơi nó có thể có tác dụng chống lại ung thư.”
Khi được tiêm liều cao nhất, 100% bệnh nhân có phản ứng miễn dịch, cho thấy vaccine có thể giúp giảm các chỉ số ung thư trong máu của bệnh nhân có dấu hiệu bệnh vẫn còn.
“Chúng tôi không mong đợi rằng chúng tôi có thể thấy tín hiệu lâm sàng như chúng tôi đã làm,” tiến sĩ Eileen O’Reilly, một bác sĩ ung thư tiêu hóa tại Trung tâm Ung thư Memorial Sloan Kettering ở New York City và tác giả chính của nghiên cứu, cho DailyMail.com biết. “Chúng tôi đã thấy rằng điều này rất khả thi. Rất an toàn, rất dễ dàng. Bệnh nhân rất yêu thích nó.”
Giai đoạn này bao gồm 25 bệnh nhân mắc ung thư tuyến tụy hoặc ruột kết.
Họ đều đã cắt bỏ khối u của mình và không có dấu hiệu ung thư trên các chụp ảnh.
Tuy nhiên, họ vẫn có các chỉ số ung thư trong máu, bao gồm DNA khối u lưu hành, hay ctDNA. Đây là DNA trực tiếp từ các tế bào ung thư.
Điều này có nghĩa là ung thư vẫn còn, dẫn đến nguy cơ khối u quay trở lại gần như không thể tránh khỏi.
“Đó là lúc mà người bị bệnh, người không may không được chữa khỏi, có lượng ung thư thấp nhất,” tiến sĩ Kasi nói.
“Những người bệnh này rất có nguy cơ. Thực ra, nguy cơ cao có lẽ không phải là thuật ngữ chính xác để thực sự biểu hiện tình hình thế nào. Đây là những bệnh nhân không được chữa khỏi sau cơ hội tốt nhất của bạn.”
Loại vaccine này nhắm vào biến đổi gen KRAS, được thấy ở bệnh nhân mắc nhiều loại ung thư khác nhau, bao gồm ung thư tuyến tụy và ruột kết.
KRAS là một gen gây ung thư, hay một gen biến đổi có khả năng gây ra ung thư.
Mạng lưới Hành động Ung thư Tuyến tụy ước tính rằng khoảng 95% bệnh nhân ung thư tuyến tụy có biến đổi gen KRAS.
“Đó gần như là phổ biến ở người mắc ung thư tuyến tụy,” tiến sĩ O’Reilly nói.
Ngoài ra, tới một nửa số bệnh nhân ung thư ruột kết có nó. Vì KRAS phổ biến ở ung thư tuyến tụy và ruột kết, các nhà nghiên cứu cảm thấy đây là những loại ung thư tốt nhất để kiểm tra loại vaccine trước tiên.
“Những loại này được chọn làm hình mẫu cho các loại ung thư có biến đổi gen KRAS,” tiến sĩ Kasi nói.
Loại vaccine này được tiêm vào cả hai cánh tay và hai chân, tổng cộng là bốn mũi tiêm mỗi tuần trong bốn tuần. Bệnh nhân tiếp tục với quá trình này mỗi hai tuần một lần trong hai tuần, sau đó tạm dừng trước khi bắt đầu một giai đoạn tăng cường kéo dài ba tháng.
Giai đoạn tăng cường là cần thiết vì sau một thời gian, phản ứng miễn dịch đối với vaccine sẽ giảm.
Đây là một loại vaccine “sẵn có”, có nghĩa là nó không được tùy biến cho từng bệnh nhân riêng lẻ.
“Có những lợi thế thực tế rất lớn đối với những loại tiếp cận này so với các loại vaccine ung thư cá nhân hóa,” tiến sĩ O’Reilly nói.
Các loại vaccine cá nhân hóa lấy các tế bào ung thư từ bệnh nhân và tạo ra một loại vaccine trong phòng thí nghiệm sử dụng các tế bào của chính bệnh nhân. Một loại vaccine cá nhân hóa yêu cầu nhiều bước tốn thời gian, bao gồm lấy mẫu khối u để gửi đến công ty vaccine để kiểm tra. Điều này dẫn đến thời gian chờ lâu hơn, cũng như chi phí cao hơn.
Trong trường hợp ung thư, tiết kiệm thời gian có thể có nghĩa là cứu sống một mạng sống.
“Một cái gì đó sẵn có là được làm sẵn và sẵn sàng đi,” tiến sĩ Kasi nói. “Nó có ý nghĩa rộng rãi hơn so với một loại vaccine cá nhân hóa.”
Trong một số nghiên cứu vaccine khác, loại vaccine được kết hợp với các loại điều trị khác, bao gồm hóa trị. Tuy nhiên, điều làm cho nghiên cứu này độc đáo là bệnh nhân chỉ được tiêm vaccine mà thôi.
Tuy nhiên, có những hạn chế. Loại vaccine này chỉ dành cho bệnh nhân có ung thư chưa lan rộng, không áp dụng cho giai đoạn III hoặc IV của bệnh.
“Không có khả năng nó sẽ có những lợi thế tương tự ở người có khối u to, triệu chứng, tiến triển. Chúng tôi cố ý nhắm vào hệ miễn dịch khi nó có khả năng cao nhất,” tiến sĩ O’Reilly nói.
Đây có thể là một nhược điểm lớn đối với ung thư tuyến tụy, ví dụ. Viện Ung thư Quốc gia (NCI) ước tính rằng hơn một nửa số ca ung thư này được chẩn đoán sau khi bệnh đã lan rộng đến các cơ quan khác vì các triệu chứng sớm, chẳng hạn như vàng da và đau bụng, dễ bị bỏ qua.
“Có một nhu cầu chưa được đáp ứng rất lớn ở các bệnh nhân tiên tiến hơn có bệnh di căn xa,” tiến sĩ Haqq nói.
Năm ngoái, hai người đồng sáng lập của công ty sản xuất thuốc BioNTech Uğur Şahin và Özlem Türeci cho biết rằng các loại vaccine để điều trị ung thư có thể có sẵn vào cuối thập kỷ này.
Ngoài loại vaccine này, hàng trăm loại vaccine khác đang được phát triển để chống lại bệnh ung thư.
Đa số các bệnh nhân trong nghiên cứu này mắc ung thư tuyến tụy, loại ung thư gây tử vong thứ ba ở Hoa Kỳ, theo NCI.
Trung bình, chỉ có 12,5% sống sót sau năm năm.
NCI ước tính sẽ có khoảng 64.000 ca ung thư tuyến tụy mới được chẩn đoán trong năm nay, cùng với hơn 50.000 ca tử vong.
Số ca mắc bệnh đang tăng. Tại Hoa Kỳ, tỷ lệ mắc bệnh đã tăng 1% mỗi năm kể từ năm 2000, theo Hiệp hội Ung thư Mỹ.
Trên toàn cầu, số ca mắc bệnh đã tăng gấp đôi kể từ năm 1990, một nghiên cứu năm 2019 trên The Lancet ước tính.
Phần còn lại của các bệnh nhân mắc ung thư ruột kết, loại ung thư tăng nhanh trên toàn cầu ở người trẻ.
Hiệp hội Ung thư Mỹ ước tính khoảng 153.000 ca ung thư ruột kết sẽ được phát hiện trong năm nay, trong đó có 19.500 ca ở những người dưới 50 tuổi.
Một số 52.550 người dự kiến sẽ chết vì bệnh này.
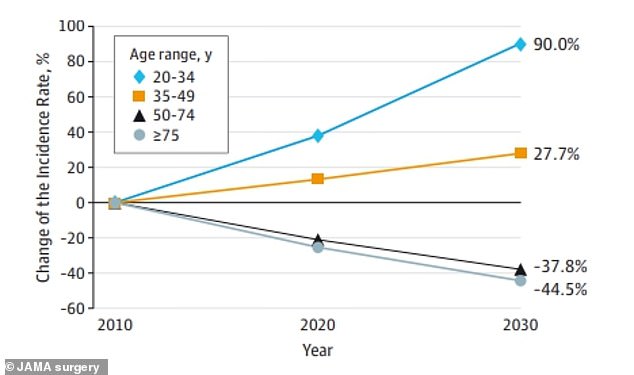
Số ca mắc bệnh dự kiến sẽ tăng gấp đôi giữa năm 2010 và 2030 ở người dưới 40 tuổi, phần lớn trong số đó được chẩn đoán ở giai đoạn muộn do các triệu chứng rộng rãi.
Các bệnh nhân trong nghiên cứu cũng ghi nhận ít triệu chứng, bao gồm đau đầu, mệt mỏi, sốt nhẹ, nhức nhối ở cánh tay và chân, và đỏ quanh vùng tiêm.
Vì vaccine đi thẳng đến hạch bạch huyết, tiến sĩ O’Reilly cho biết rằng điều này có thể giúp tránh các tác dụng phụ nghiêm trọng hơn, như sốt cao và run rẩy.
Kết quả của nghiên cứu vẫn cần được xác nhận, nhưng các nhà nghiên cứu đã bắt đầu tuyển dụng hàng trăm bệnh nhân cho giai đoạn tiếp theo.
Trong khi giai đoạn ban đầu tập trung vào hai peptit, giai đoạn này sẽ sử dụng bảy peptit.
Tiến sĩ O’Reilly so sánh cơ chế hoạt động của vaccine với một bộ Lego. Trong các giai đoạn tiếp theo, thêm nhiều peptit có thể được gắn vào vaccine, nhắm vào nhiều biến đổi khác nhau.
“Với hệ thống giao hàng nền tảng này, tiến lên, các kháng nguyên khác có thể được gắn vào như các mục tiêu khác cho hệ miễn dịch,” tiến sĩ O’Reilly nói.
“Điều đó làm cho nó rất có thể mở rộng, rất dễ sản xuất và rất dễ tiêm.”
Mục tiêu của giai đoạn tiếp theo là “xác nhận tất cả những gì chúng tôi đã học được cho đến nay,” bà nói.
Giai đoạn này dự kiến sẽ diễn ra vào cuối năm nay, với việc tuyển dụng ước tính mất khoảng sáu tháng.
Các giai đoạn bổ sung sẽ nhắm vào năm loại ung thư khác có thể có biến đổi gen KRAS, bao gồm ung thư túi mật, buồng trứng và phổi.
“Khả năng áp dụng trong tương lai có thể là cho rất nhiều loại ung thư khác có biến đổi gen KRAS,” tiến sĩ Kasi nói.
Các tác giả nhấn mạnh rằng nghiên cứu này vẫn còn sơ khai và có thể mất nhiều năm trước khi phương pháp điều trị này trở thành tiêu chuẩn.
Nhưng họ hy vọng rằng nó sẽ tiếp tục mang lại kết quả ấn tượng.
“Nếu điều này được duy trì, hy vọng là chúng tôi sẽ giảm nguy cơ tái phát sau khi cắt bỏ và rằng mọi người sẽ sống lâu hơn không bị ung thư và có tỷ lệ sống sót được cải thiện,” tiến sĩ O’Reilly nói.
“Đây là một thời điểm thú vị,” tiến sĩ Kasi nói.
Dịch bởi Phương Quyên & nhóm tại Đại Học Stanford (USA).
Nguồn tham khảo
- Bortz D. EXCLUSIVE: Are we on the verge of vaccinating against CANCER?¹[1] Another promising shot treats two of the deadliest and fastest-rising forms of the disease, early study shows [Internet]²[2]. Mail Online. 2021 [cited 2023 Jul 14]. Available from: https://www.dailymail.co.uk/health/article-12162513/Promising-vaccine-treat-two-deadliest-fastest-rising-forms-cancer-early-study-shows.html
- Pancreatic Cancer Action Network. KRAS Gene Mutation [Internet]. 2020 [cited 2023 Jul 14]. Available from: https://www.pancan.org/facing-pancreatic-cancer/diagnosis/staging/kras-gene-mutation/
- American Cancer Society. Key Statistics for Pancreatic Cancer [Internet]. 2021 [cited 2023 Jul 14]. Available from: https://www.cancer.org/cancer/pancreatic-cancer/about/key-statistics.html
- Rawla P, Sunkara T, Gaduputi V. Epidemiology of Pancreatic Cancer: Global Trends, Etiology and Risk Factors. World J Oncol. 2019;10(1):10-27.
- American Cancer Society. Colorectal Cancer Facts & Figures 2020-2022 [Internet]. 2020 [cited 2023 Jul 14]. Available from: https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/colorectal-cancer-facts-and-figures/colorectal-cancer-facts-and-figures-2020-2022.pdf
- Arnold M, Sierra MS, Laversanne M, Soerjomataram I, Jemal A, Bray F. Global patterns and trends in colorectal cancer incidence and mortality. Gut. 2017;66(4):683-691.
- National Cancer Institute. Pancreatic Cancer Treatment (PDQ®)–Patient Version [Internet]. 2021 [cited 2023 Jul 14]. Available from: https://www.cancer.gov/types/pancreatic/patient/pancreatic-treatment-pdq
- National Cancer Institute. Colon Cancer Treatment (PDQ®)–Patient Version [Internet]. 2021 [cited 2023 Jul 14]. Available from: https://www.cancer.gov/types/colorectal/patient/colon-treatment-pdq
- O’Reilly EM, Kasi PM, Haqq C, et al. A phase Ib study of a novel KRAS vaccine (Elicio-001) in patients with locally advanced or metastatic pancreatic or colorectal cancer with a KRAS G12D or G12V mutation who have completed first-line therapy [abstract]. In: Proceedings of the American Association for Cancer Research Annual Meeting 2021; 2021 Apr 10-15 and May 17-21. Philadelphia (PA): AACR; Cancer Res 2021;81(13 Suppl):Abstract nr CT002.
Tìm kiếm:
- Vaccine ung thư mới nhắm vào biến đổi gen KRAS có thể cải thiện tỷ lệ sống sót cho ung thư ruột kết và tuyến tụy
- Vaccine ung thư sử dụng albumin để kích hoạt hệ miễn dịch cho thấy kết quả khả quan trong nghiên cứu sơ bộ
- Vaccine ung thư không cần tùy biến cho từng bệnh nhân có thể giảm nguy cơ tái phát bệnh ở ung thư ruột kết và tuyến tụy
- Vaccine ung thư đầu tiên nhắm vào biến đổi gen KRAS cho thấy hiệu quả trong nghiên cứu trên người
- Vaccine ung thư “hạ cánh” trên hạch bạch huyết có thể giúp chống lại hai loại ung thư tăng nhanh nhất
- Vaccine ung thư mới có khả năng giảm các chỉ số ung thư trong máu của bệnh nhân mắc ung thư ruột kết và tuyến tụy
- Vaccine ung thư “thuần khiết” chỉ sử dụng peptit để kích hoạt hệ miễn dịch cho thấy lợi thế so với các loại vaccine cá nhân hóa
- Vaccine ung thư mới có tiềm năng điều trị năm loại ung thư khác có biến đổi gen KRA